豆漿加醋為什麼會結塊?化學解密鹹豆漿之謎
文章來源 : PanSci 泛科學
撰文= 白尾
原文連結 : https://pansci.asia/archives/167211
平凡的一天早晨,來點熟悉的鹹豆漿最對味,但,問題來了:到底為什麼豆漿加了醋後,就會產生塊狀物,變成好吃(喝)的鹹豆漿呢?在與泛糰們互動的過程中,我們發現資料中出現了不同的說法,因此,便有位泛糰認真地開始研究這個問題,並將他的理解與我們分享。
豆漿豆漿,你為何會變得不一樣?
關於「鹹豆漿加醋為什麼會產生塊狀物?」這個問題,在搜尋眾多的網路資料後,會發現主要有兩派說法:
- 因為加入了電解質,讓豆漿中膠體粒子的正負電荷相等,呈電中性,進而產生凝聚。
- 因為加入酸性物質,讓豆漿中的蛋白質變性,進而產生凝聚。
以上兩種說法,看似都說得通,但難免讓人想知道:何者才是正確的原因呢?

豆漿、牛奶都是我們日常生活中常見的膠體。圖/pxhere
在深入討論前,我們首先要了解什麼是「膠體」。
膠體 (Colloid) 是一種由兩種不同物質混合而成的均勻混合物。形成膠體時,並不會像鹽溶於水一樣,發生溶解作用。常見的膠體有:霧、果凍、牛奶,當然還有今天的主角──豆漿。
而說到鹹豆漿凝聚的過程,我們要先談談膠體的其中一個特性:帶電。
膠體之所以可以均勻混合,除了微小粒子間不斷碰撞的布朗運動之外,另一個原因就是帶電。膠體粒子外有所謂電雙層 (electrical double-layer) 的結構,藉由電性相斥,讓其中的膠體粒子不會互相結合凝聚。而豆漿中的膠體粒子主要是蛋白質,帶負電荷。
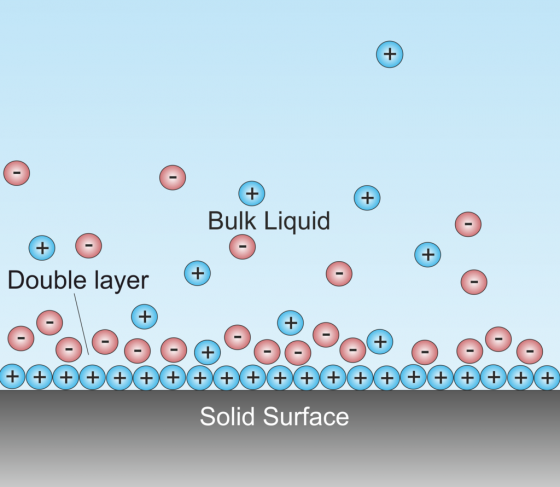
電雙層的機制能讓膠體溶液中的膠體粒子不會互相結合凝聚。圖/wikipedia
豆皮豆腐鹹豆漿,凝聚方法不一樣
那麼,豆漿裡的蛋白質到底要怎樣才會凝聚呢?主要有三個方法:加熱、加鹽類、改變 pH值。剛好,這三個方法可以依序對應到我們常吃到的三種豆類食品:豆皮、豆腐、鹹豆漿。
加熱時,蛋白質之間會產生雙硫鍵,互相連結,而在冷卻的過程中,氫鍵則扮演了強化結構的角色。
如果大家想自己在家做豆皮,只要加熱豆漿,等表面形成薄膜之後小心撈出晾乾即可。不過,有一點要注意的是:製作豆皮要用小火,不能讓豆漿沸騰,否則就無法在表面形成完整的薄膜。
加鹽類與酸可以直接讓蛋白質凝聚,而在製作豆腐及鹹豆漿之前,通常也會先透過加熱讓蛋白質變性,這個步驟可以讓蛋白質的疏水基暴露出來,使其更容易凝聚。
加熱後的豆漿,若加入鹽滷(主要成分為氯化鎂)或石膏(主要成分為硫酸鈣)等鹽類,再經過一段時間的排水、成型,就完成豆腐了。
若加入的是醋及其他佐料,經過攪拌即成鹹豆漿。
我們可從下圖看出,加酸及加鹽類分別是兩條不同的路徑:
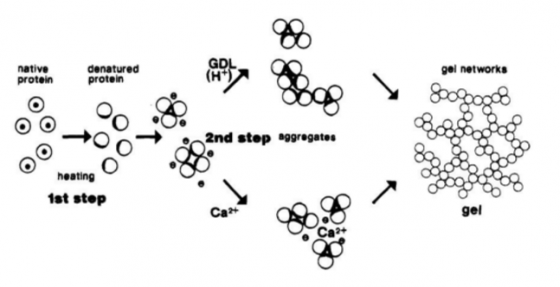
GDL 即葡萄糖酸內酯,溶於水中呈酸性,可用來製作豆花、嫩豆腐。
圖片來源:Elise Ringgenberg (2011)
加鹽 vs. 加酸,凝聚機制有什麼不一樣?
在上一段我們將「加鹽類」和「加酸」分成了兩個類別,但它們到底有什麼差別呢?接下來,就要仔細說明一下兩者間的不同。
加鹽類:
豆漿加入鹽類後,鹽類中帶正電的鈣、鎂離子會中和蛋白質膠體粒子表面所帶的負電,讓膠體粒子呈電中性。此時,膠體粒子失去了電荷的排斥作用,互相碰撞後便會凝聚在一起。
當單一離子帶有的電荷越多,要達到凝聚所需加入的量就會越少。此外,相同價數的離子也會有不同的效果,例如:鈣的凝聚效果便比鎂來得好。
豆漿中的蛋白質膠體粒子帶負電荷,主要由鹽類中的正離子來中和,而鹽類中的負離子種類,也會影響凝聚所需的量,如氯鹽的凝聚效果便比硫酸鹽好。
90 年的大學聯考題曾有一題:「加食鹽會不會讓豆漿凝聚?」
當時大考中心給的答案是「會」,不過,由於鈉離子跟鈣相比,需要非常多的量才能達到凝聚的效果──在 As2S3 膠體(此膠體粒子帶負電)中加入氯化鈉(NaCl,食鹽)及氯化鈣(CaCl2)測定凝聚產生需要的最小濃度,結果分別為 51 及 0.65 mmol/L,由此可見,鹹豆漿裡面的鈉不是主要讓蛋白質凝聚的主要因素 (不然會鹹死) 。
加酸:
在了解加入酸會發生什麼事之前,需要了解一個詞:等電點。
等電點指的是一個兩性離子達到電中性時的 pH值。兩性離子(兩性分子的離子態)的特點是同時具有正負電荷,大部分的胺基酸便是兩性分子的一種。
豆漿裡面的兩種主要蛋白 Glycinin、beta-Conglycinin,等電點約在 5 左右(變性的蛋白質其等電點會稍微改變,但變化不大)。一旦加入酸,便會讓此二蛋白質膠體粒子趨近於等電點;越接近等電點,膠體粒子的淨電荷數越少,意味著膠體粒子間的斥力越小,便越容易凝聚。
綜合所述,可以得知:加鹽類跟改變 pH值,其實都是在改變膠體粒子的淨電荷數,原理上並沒有太多的區別。

鹹豆漿的謎團就讓我們一同解開。圖/wikimedia
以上講了那麼多,鹹豆漿之謎的解答到底是什麼呢?或許,我們可以整理出一個比較精確的敘述——
經過加熱的變性蛋白質膠體粒子,加醋之後,降低了表面的淨電荷數量,讓膠體粒子在接觸時容易互相凝聚;而因蛋白質變性所露出的疏水基,讓凝聚作用能進行得更加順利。
參考資料:
- 施建輝(2014)。膠體溶液的帶電性與凝聚。台灣化學教育
- Ringgenberg, E. (2011). The Physico-Chemical Characterization of Soymilk Particles and Gelation Properties of Acid-Induced Soymilk Gels, as a Function of Soymilk Protein Concentration (Doctoral dissertation).
- Li Tay, S., Yao Tan, H., & Perera, C. (2006). The coagulating effects of cations and anions on soy protein. International journal of food properties, 9(2), 317-323.
- Ui, N. (1973). Conformational studies on proteins by isoelectric focusing. Annals of the New York Academy of Sciences, 209(1), 198-209.
以上內容分享於 PanSci 泛科學 。所有資訊不代表本公司立場,內容及版權歸該媒體所有

